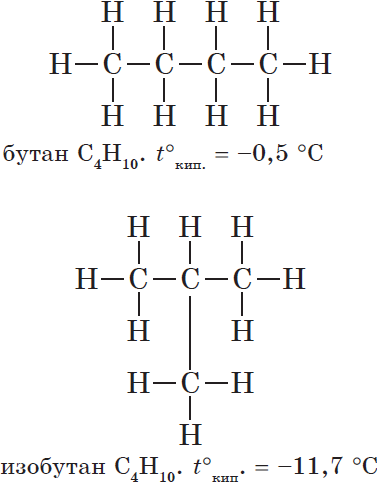
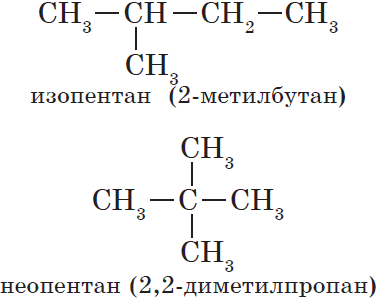
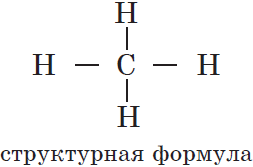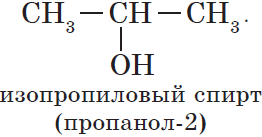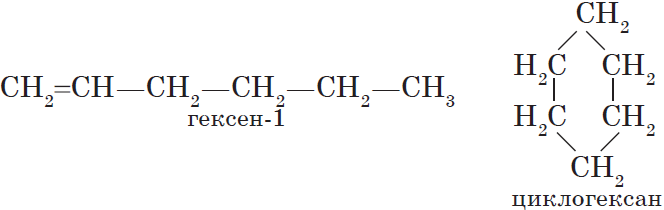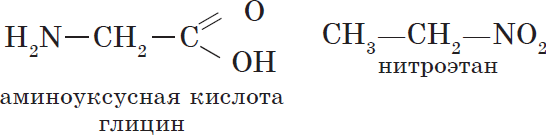что такое гомология органических соединений
Гомология органических соединений
Полезное
Смотреть что такое «Гомология органических соединений» в других словарях:
Гомология в химии — Гомология органических соединений, или закон гомологов, состоит в том, что вещества одной химической функции и одинакового строения, отличающиеся друг от друга по своему атомному составу лишь на nCH2, оказываются сводными и во всем своем… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Гомология (биология) — У этого термина существуют и другие значения, см. Гомология. Гомологичные кости (показаны цветом) передних конечностей человека, собаки, птицы и кита. Гомологичным … Википедия
Ортолог — Гомологичными (от др. греч. ὅμοιος «подобный, похожий» и др. греч. λογος «слово», «закон») называют сопоставимые части сравниваемых объектов. В биологии понятие гомологии используется в сравнительной анатомии с середины XIX века, и в… … Википедия
Паралог — Гомологичными (от др. греч. ὅμοιος «подобный, похожий» и др. греч. λογος «слово», «закон») называют сопоставимые части сравниваемых объектов. В биологии понятие гомологии используется в сравнительной анатомии с середины XIX века, и в… … Википедия
Уменьшение числа гомологичных органов — Гомологичными (от др. греч. ὅμοιος «подобный, похожий» и др. греч. λογος «слово», «закон») называют сопоставимые части сравниваемых объектов. В биологии понятие гомологии используется в сравнительной анатомии с середины XIX века, и в… … Википедия
Гомологический ряд — Рис. 1 Температуры плавления (синий) и кипения (красный) в гомологическом ряду n алканов C1…C14 … Википедия
Углеводороды — (хим.). У. называются соединения, заключающие только углерод и водород. По способности к соединению с водородом углероду принадлежит совершенно исключительное положение среди всех металлоидов. Действительно, в то время, как для галоидов (фтора,… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
гомологический — (гр. homologos соответственный, подобный) однозначащий, имеющий одинаковое отношение к чему л.; сходный; г ие ряды хим. группы органических соединений, отдельные члены которых (гомологи) отличаются друг от друга на одну или больше метиленовых… … Словарь иностранных слов русского языка
Теория строения органических соединений: гомология и изомерия (структурная и пространственная). Взаимное влияние атомов в молекулах
Содержание:
Что такое органическая химия?
Органическая химия – это раздел химии, который изучает структуру, свойства и методы получения (синтеза) углеводородов и их производных. Сейчас число известных органических соединений составляет почти 30 млн, однако оно продолжает расти (в мае 1999 года было известно около 12 млн органических веществ). Этот рост обусловлен необычными свойствами углерода. Например, данный элемент может образовать цепи любой длины, способные замыкаться и образовывать циклы, а также атом углерода способен создавать одинарные, двойные или тройные связи. Валентность углерода всегда равна 4-м, поэтому он всегда будет создавать вокруг себя 4 связи. Это могут быть четыре одинарных, две двойных, одна тройная и одна одинарная и др. В любом случае, способов образовывать связи много, однако чаще всего углерод связывается с водородом, кислородом, фосфором, азотом и некоторыми другими атомами этих элементов.
Теория строения органических соединений
Ещё в глубокой древности люди могли получать органические вещества, но теория их строения была сформулирована только в 1860-х годах русским химиком Александром Михайловичем Бутлеровым. Теория получила название в честь своего автора и стала фундаментом органической химии. До возникновения этой теории существовала такая точка зрения, что органические вещества нельзя получить из неорганических, то есть для их синтеза необходима некая сила, существующая только у живых организмов. Естественно, что появление теории, противоречащей всем знаниям в области органики, вызвало непонимание у химиков того времени. Научившись самостоятельно синтезировать органические вещества, ученые столкнулись с соединениями с одинаковой молекулярной формулой и молярной массой, но абсолютно другими свойствами. Например, диметиловый эфир при нормальных условиях представляет собой газ, а этиловый спирт, имеющий такой же состав, – жидкость. Подобные соединения стали называть изомерами, а явление – изомерией.
Основные положения теории Бутлерова
Данная теория оказала сильное влияние на скорость развития органической химии. С ее помощью А.М. Бутлеров объяснил явление изомерии, а также самостоятельно получил некоторые изомеры, в очередной раз доказав верность своих мыслей.
Гомология и изомерия.
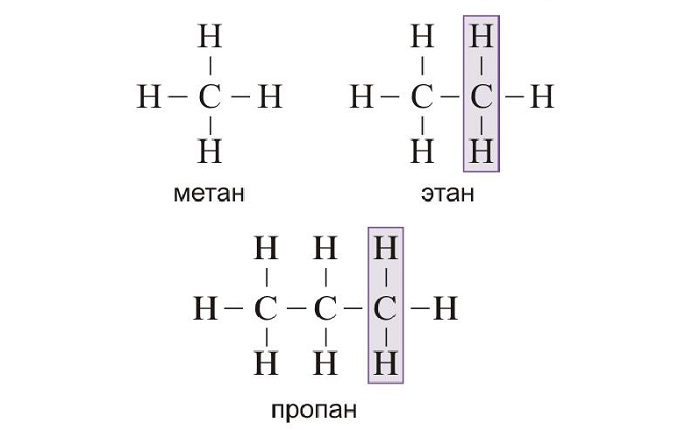
Гомология (от греч. «подобный») – явление, при котором вещества имеют похожие строение и свойства, но отличаются между собой по молекулярному составу на одну или несколько групп CH2. Например алканы: CH4(метан), C2H6(этан), C3H8(пропан), C4H10(бутан). В органической химии существуют целые гомологические ряды. У каждого класса органических веществ есть свой гомологический ряд, отражающий общую формулу соединений, входящих в него.
Гомологический ряд алканов
Формула
Название вещества
Изомерия (от греч. «равный») – явление, при котором вещества имеют похожий количественный и качественный состав, но разные строение и свойства. Изомерия бывает структурная и пространственная.
Структурная изомерия
Структурные изомеры – вещества одинакового количественного и качественного состава, но разного химического строения. Структурная изомерия бывает 3-х типов.
Изомерия углеродного скелета
(В 1-м случае CH3 – часть углеродной цепи, а во 2-м – радикал).
Изомерия положения
(Меняется положение двойной связи. В 1-м случае двойная связь у первого атома углерода, а во 2-м – у второго).
2.2 функциональной группы
(Меняется положение гидроксогруппы от 1-го атома углерода ко 2-му).
(Меняется положение атома хлора (галогена) от 1-го атома углерода ко 2-му).
Межклассовая изомерия
(Меняется класс вещества).
Пространственная изомерия
Пространственные изомеры (стереоизомеры) – вещества одинакового количественного и качественного состава и одинакового химического строения, отличающихся друг от друга пространственным расположением атомов в молекуле. Пространственная изомерия бывает 2-х типов.
Геометрическая изомерия
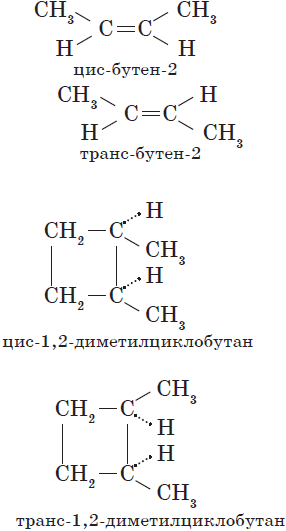
Встречается у веществ, имеющих цикл или двойную (С=С) связь. Данный вид пространственной изомерии еще называют цис – и – транс изомерией.
(Атом водорода и группа CH3 меняются местами).
Оптическая изомерия
Суть оптической изомерии заключается в том, что если атом углерода в молекуле связан с 4-мя различными атомами или атомными группами, то из него можно получить два соединения с одинаковой структурой, молекулы которых будут являться зеркальными копиями друг друга (как правая и левая руки человека). В пример можно привести D-глюкозу и L-клюкозу.
Взаимное влияние атомов в молекулах
С момента появления электронной теории химической связи (1912-1916 гг.) знания о структуре химических соединений, как о последовательности соединенных атомов, были значительно пополнены. Данная теория объясняет причину влияния атомов или групп атомов внутри молекулы друг на друга. Всего существует два способа такого взаимодействия.
Индуктивный эффект
Мезомерный эффект
Заключение
Органическая химия играет большую роль в существовании живых организмов. С давних времен люди пытались разгадать тайны органических веществ, но стремительно развиваться этот раздел химии начал только в середине XIX века. Разгадав тайны строения этих соединений, люди продолжили двигаться вперед, открывая новое и в большинстве случаях полезное для человечества (например, препарат пенициллин). Прочитав данную статью, вы узнали о теории А.М. Бутлерова, о таких явлениях как гомология и изомерия и о взаимном влиянии атомов в молекулах. Все эти открытия, сделанные людьми несколько столетий назад, являются основами органической химии по сей день.
Например, если говорить о гомологическом ряде алкинов, он состоит из следующих гомологов:
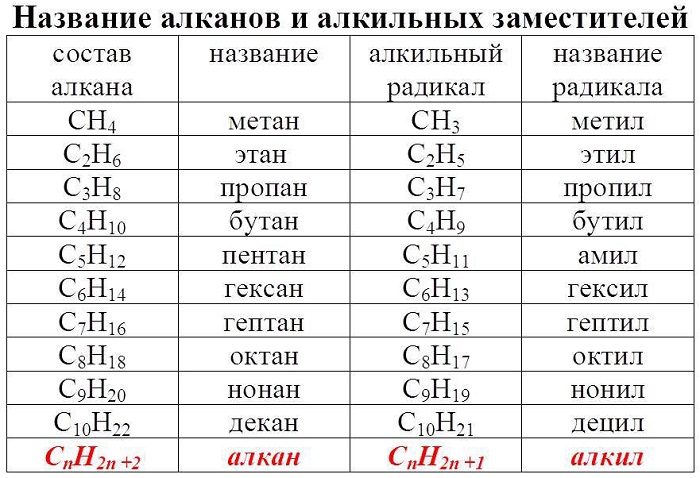
Гомологический ряд алканов в таблице
Алканы обладают следующими свойствами:
в последовательности гомологического ряда происходят изменения агрегатных состояний веществ с газообразного на жидкое и на твёрдое;
нерастворимы в воде, но могут растворяться в неполярных растворителях;
Алканы могут вступать в следующие реакции:
Замещение с галогенами: CH4 + Cl2 = CH3Cl + HСl.
Разложение при высокой температуре: СН4 = C + 2H2.
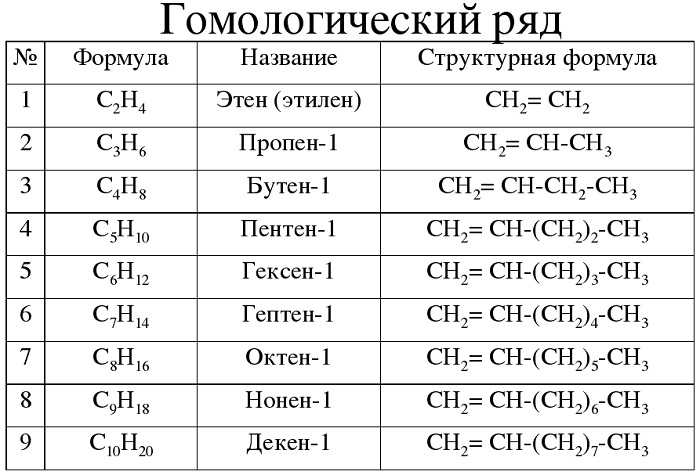
Гомологический ряд алкенов в таблице
Алкены обладают следующими свойствами:
не способны растворяться в воде, но полностью растворяются при взаимодействии с органическими растворителями;
имеют очень высокую температуру плавления и кипения;
применяются в промышленности для синтеза таких важных соединений, как фенола, полипропилена, стирола, ацетона, глицерина и других.
Алкены участвуют в следующих химических реакциях:
Галогенирование (присоединение к галогенам): CH2=CH2 + Cl2 = Cl-CH2-CH2-Cl.
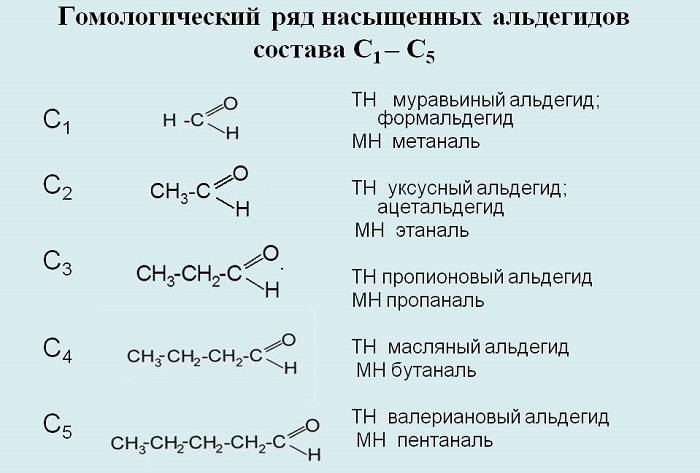
Гомологический ряд альдегидов
К примерам альдегидов относятся метаналь, этаналь, пропаналь, бутаналь, пентаналь, гексаналь и так далее.
Альдегиды принимают участие в следующих реакциях:
Присоединение воды: R-CH = O + H2O = R-CH(OH)-OH.
Восстановление водородом: R-CH = O + H2 = R—CH2-OH.
Альдегиды обладают следующими свойствами:
низшие представители класса имеют резкий запах;
в гомологическом ряду происходит изменение агрегатных состояний от жидкого до твёрдого;
используются в лекарственной промышленности, парфюмерии и т. д.
Хоть органическая химия и требует внимательного изучения, совсем необязательно полностью зазубривать все классы веществ. Намного проще для понимания и качественного запоминания обращать внимание именно на закономерности изменения свойств и характеристик ближайших соединений, следуя плану.
Теория строения органических соединений. Типы связей в молекулах органических веществ
Теория к заданию 12 из ЕГЭ по химии
Теория строения органических соединений: гомология и изомерия (структурная и пространственная). Взаимное влияние атомов в молекулах
Теория химического строения органических соединений А. М. Бутлерова
Подобно тому, как для неорганической химии основой развития являются Периодический закон и Периодическая система химических элементов Д. И. Менделеева, для органической химии основополагающей стала теория строения органических соединений А. М. Бутлерова.
Основным постулатом теории Бутлерова является положение о химическом строении вещества, под которым понимается порядок, последовательность взаимного соединения атомов в молекулы, т.е. химическая связь.
Под химическим строением понимают порядок соединения атомов химических элементов в молекуле согласно их валентности.
Основные положения теории А. М. Бутлерова
Теория строения органических соединений является динамичным и развивающимся учением. По мере развития знаний о природе химической связи, о влиянии электронного строения молекул органических веществ стали пользоваться, кроме эмпирических и структурных, электронными формулами. В таких формулах указывают направление смещения электронных пар в молекуле.
Квантовая химия и химия строения органических соединений подтвердили учение о пространственном направлении химических связей (цис- и трансизомерия), изучили энергетические характеристики взаимных переходов у изомеров, позволили судить о взаимном влиянии атомов в молекулах различных веществ, создали предпосылки для прогнозирования видов изомерии и направления и механизма протекания химических реакций.
Органические вещества имеют ряд особенностей:
Изомерия и гомология органических веществ
Свойства органических веществ зависят не только от их состава, но и от порядка соединения атомов в молекуле.
Изомерия — это явление существования разных веществ — изомеров с одинаковым качественным и количественным составом, т.е. с одинаковой молекулярной формулой.
Различают два вида изомерии: структурную и пространственную (стереоизомерию). Структурные изомеры отличаются друг от друга порядком связи атомов в молекуле; стереоизомеры — расположением атомов в пространстве при одинаковом порядке связей между ними.
Выделяют следующие разновидности структурной изомерии: изомерию углеродного скелета, изомерию положения, изомерию различных классов органических соединений (межклассовую изомерию).
Структурная изомерия
Изомерия положения обусловлена различным положением кратной связи, заместителя, функциональной группы при одинаковом углеродном скелете молекулы:
Изомерами являются углеводород, относящийся к алкинам, — бутин-1 и углеводород с двумя двойными связями в цепи бутадиен-1,3:
Изомеры этого типа содержат различные функциональные группы и относятся к разным классам веществ. Поэтому они отличаются по физическим и химическим свойствам значительно больше, чем изомеры углеродного скелета или изомеры положения.
Пространственная изомерия
Пространственная изомерия подразделяется на два вида: геометрическую и оптическую. Геометрическая изомерия характерна для соединений, содержащих двойные связи, и циклических соединений. Так как свободное вращение атомов вокруг двойной связи или в цикле невозможно, заместители могут располагаться либо по одну сторону плоскости двойной связи или цикла (цис-положение), либо по разные стороны (транс-положение). Обозначения цис- и транс- обычно относят к паре одинаковых заместителей:
Геометрические изомеры различаются по физическим и химическим свойствам.
Изучение оптической изомерии необходимо при рассмотрении многих реакций, протекающих в организме. Большинство этих реакций идет под действием ферментов — биологических катализаторов. Молекулы этих веществ должны подходить к молекулам соединений, на которые они действуют, как ключ к замку, следовательно, пространственное строение, взаимное расположение участков молекул и другие пространственные факторы имеют для течения этих реакций большое значение. Такие реакции называются стереоселективными.
Большинство природных соединений являются индивидуальными энантиомерами, и их биологическое действие резко отличается от свойств их оптических антиподов, полученных в лаборатории. Подобное различие в биологической активности имеет огромное значение, так как лежит в основе важнейшего свойства всех живых организмов — обмена веществ.
Типы связей в молекулах органических веществ. Гибридизация атомных орбиталей углерода. Радикал. Функциональная группа.
Типы связей в молекулах органических веществ.
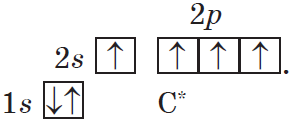
Такой атом имеет четыре неспаренных электрона и может принимать участие в образовании четырех ковалентных связей.
Характеристики одинарных и кратных связей между атомами С.
| Молекула | Тип гибридизации | Валентный угол | Длина связи, нм | Энергия связи, кДж/моль |
| $CH_3-CH_3$ | $sp^3$ | $109°5’$ | $0.154$ | $369$ |
| $CH_2=CH_2$ | $sp^2$ | $120°$ | $0.134$ | $712$ |
| $CH≡CH$ | $sp^3$ | $180°$ | $0.120$ | $962$ |
Радикал. Функциональная группа.
Одной из особенностей органических соединений является то, что в химических реакциях их молекулы обмениваются не отдельными атомами, а группами атомов. Если эта группа атомов состоит только из атомов углерода и водорода, то она называется углеводородным радикалом, если же она имеет атомы других элементов, то она называется функциональной группой. Так, например, метил ($СН_3$—) и этил ($С_2Н_5$—) являются углеводородными радикалами, а оксигруппа (—$ОН$), альдегидная группа (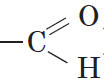
Как правило, функциональная группа определяет химические свойства органического соединения и поэтому является основой их классификации.
Урок №27. Основные классы органических соединений. Гомологические ряды
В основу классификации органических веществ положены различия в строении углеродных цепей. В соответствии с этим все органические вещества делятся на ациклические и циклические.
Ациклические (алифатические) – соединения с открытой (незамкнутой) цепью углеродных атомов.
Ациклические соединения, в свою очередь, подразделяются на
Непредельные (алкены, алкины, диеновые углеводороды)
Циклические – соединения, в молекулах которых углеродные атомы замкнуты в кольцо.
Карбоциклические – если цикл образован только углеродными атомами,
Гетероциклические – если в состав цикла помимо углеродных атомов входят атомы других химических элементов (азота, кислорода, серы)
Карбоциклические соединения, в свою очередь, подразделяются алициклические (циклоалканы) и ароматические (соединения, содержащие в составе молекулы одно или несколько бензольных колец).
Классификация органических соединений по строению углеродной цепи представлена в следующей таблице.
Углерод соединяется друг с другом одинарными и кратными связями (двойными и тройными), образуя прямые, разветвлённые и замкнутые цепи.
А) Прямая (неразветвлённая) цепь:
СH 2 = CH – CH 2 – CH 3
CH 2 = CH – CH = CH 2
Б) Разветвлённая цепь:
К циклическим относятся карбоциклические – содержащие в цикле только атом ы углерода и гетероциклические соединения – содержащие в цикле кроме атомов углерода атомы других элементов – кислорода, азота и др.
Функциональные производные углеводородов
Функциональная группа – структурный фрагмент молекулы, единый для конкретного гомологического ряда и определяющий характерные химические свойства данного класса соединений.
Примером гомологического ряда может служить ряд предельных углеводородов (алканов).
Формула любого последующего гомолога может быть получена прибавлением к формуле предыдущего углеводорода гомологической разности.
Гомологические ряды могут быть построены для всех классов органических соединений. Зная свойства одного из членов гомологического ряда, можно сделать выводы о свойствах других представителей того же ряда. Это обусловливает важность понятия гомологии при изучении органической химии.